近日,大連化物所本草物質(zhì)科學(xué)研究室(二十八室)卿光焱研究員等與大連醫(yī)科大學(xué)附屬第一醫(yī)院重癥醫(yī)學(xué)科主任萬獻(xiàn)堯團(tuán)隊(duì)合作,在膿毒癥治療領(lǐng)域取得新進(jìn)展。合作團(tuán)隊(duì)研發(fā)出一種基于多肽與分子印跡的“雙親和”材料,能夠高效捕獲并清除血液中的致命脂多糖,為膿毒癥治療提供了新路徑。
膿毒癥是一種由感染引起的全身炎癥反應(yīng)的疾病,致死率高,治療成本高昂,是臨床面臨的一大挑戰(zhàn)。脂多糖(又稱內(nèi)毒素)作為膿毒癥的核心致病因子,在疾病早期及時(shí)清除對(duì)于阻斷病情惡化、挽救患者生命至關(guān)重要。然而,由于脂多糖結(jié)構(gòu)多樣、血液中含量極低且血液成分復(fù)雜,實(shí)現(xiàn)其高效、高特異性清除一直是臨床面臨的挑戰(zhàn)。
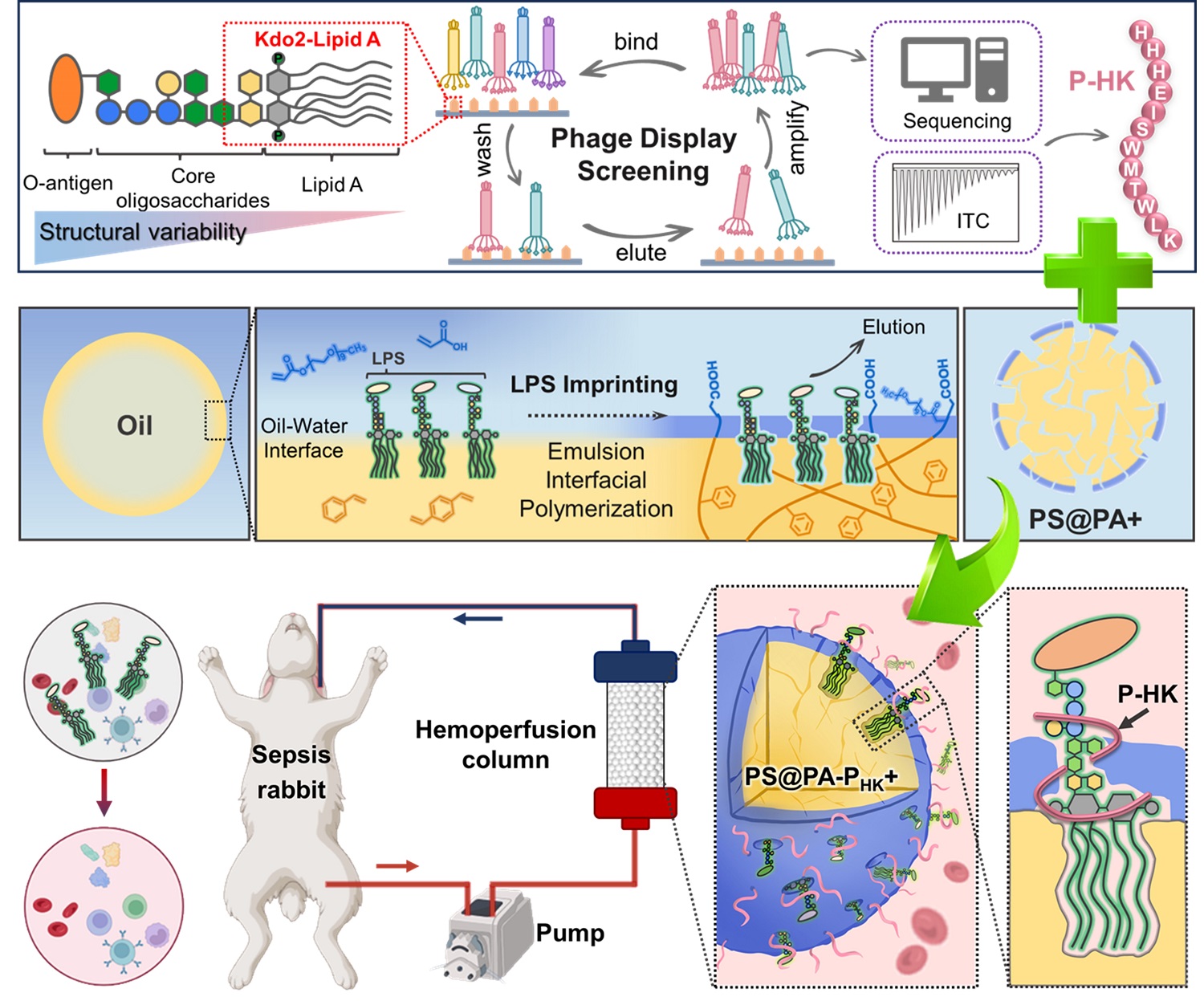
為解決上述難題,研究團(tuán)隊(duì)創(chuàng)新性地融合高親和多肽與分子印跡聚合物技術(shù),開發(fā)出新型“雙親和”脂多糖捕獲材料。團(tuán)隊(duì)首先利用脂多糖的保守結(jié)構(gòu)核心——Kdo?-Lipid A作為靶標(biāo),通過噬菌體展示技術(shù)篩選出一種新型高親和肽(P-HK),該肽對(duì)多種細(xì)菌來源的脂多糖均表現(xiàn)出較強(qiáng)的結(jié)合能力。進(jìn)一步,團(tuán)隊(duì)利用脂多糖的兩親性質(zhì),通過乳液界面聚合的方法,構(gòu)建了表面具有脂多糖精準(zhǔn)匹配空腔的印跡聚合物顆粒。最終,團(tuán)隊(duì)通過將印跡聚合物與親和肽偶聯(lián),實(shí)現(xiàn)了“形狀選擇性識(shí)別”與“肽特異性親和”的協(xié)同增效,形成獨(dú)特的“雙親和”捕獲機(jī)制。實(shí)驗(yàn)結(jié)果顯示,該材料在對(duì)大腸桿菌脂多糖的清除中,不僅在緩沖液中清除率達(dá)到99.2%,在全血環(huán)境中也保持了95.4%的高效清除性能,并對(duì)多種致病菌脂多糖均表現(xiàn)出廣譜清除能力。此外,該材料具備優(yōu)異的抗蛋白黏附性能和良好的生物相容性,可為血液凈化應(yīng)用提供關(guān)鍵安全保障。在膿毒癥兔模型治療中,基于該材料的血液灌流實(shí)現(xiàn)了84.8%的脂多糖清除率,有效緩解了多器官損傷,提升了兔的存活率。該研究有望為膿毒癥治療提供一種精準(zhǔn)、高效的技術(shù)方案。
卿光焱等一直致力于開發(fā)生物分離分析新材料、新方法,系統(tǒng)性地提出了生物分子響應(yīng)性聚合物的設(shè)計(jì)理念(Interdiscip. Mater.,2024),開發(fā)了針對(duì)脂多糖的精準(zhǔn)捕獲瓶刷狀聚合物材料(Adv. Mater.,2023)、捕獲循環(huán)腫瘤細(xì)胞的細(xì)胞印跡水凝膠(Adv. Mater.,2024)、SUMO-1修飾人工識(shí)別材料(Chem. Sci.,2025)、N-磷酸化蛋白富集磁性微球(Chem. Sci.,2025)等。
相關(guān)研究成果以“Unique Dual-Affinity Strategy for Specific Lipopolysaccharide Clearance in Sepsis Therapy: Peptide-Conjugated Molecularly Imprinted Polymers via Emulsion Interfacial Polymerization”為題,于近日發(fā)表在《先進(jìn)材料》(Advanced Materials)上。該工作的第一作者是大連化物所博士研究生魏海潔。上述工作得到了國(guó)家自然科學(xué)基金、國(guó)家重點(diǎn)研發(fā)計(jì)劃、大連化物所創(chuàng)新基金,大連醫(yī)科大學(xué)附屬第一醫(yī)院-中國(guó)科學(xué)院大連化學(xué)物理研究所醫(yī)工聯(lián)合創(chuàng)新基金等項(xiàng)目的資助。